打破 250 nm 壁垒
从"模糊轮廓"到"精细结构"
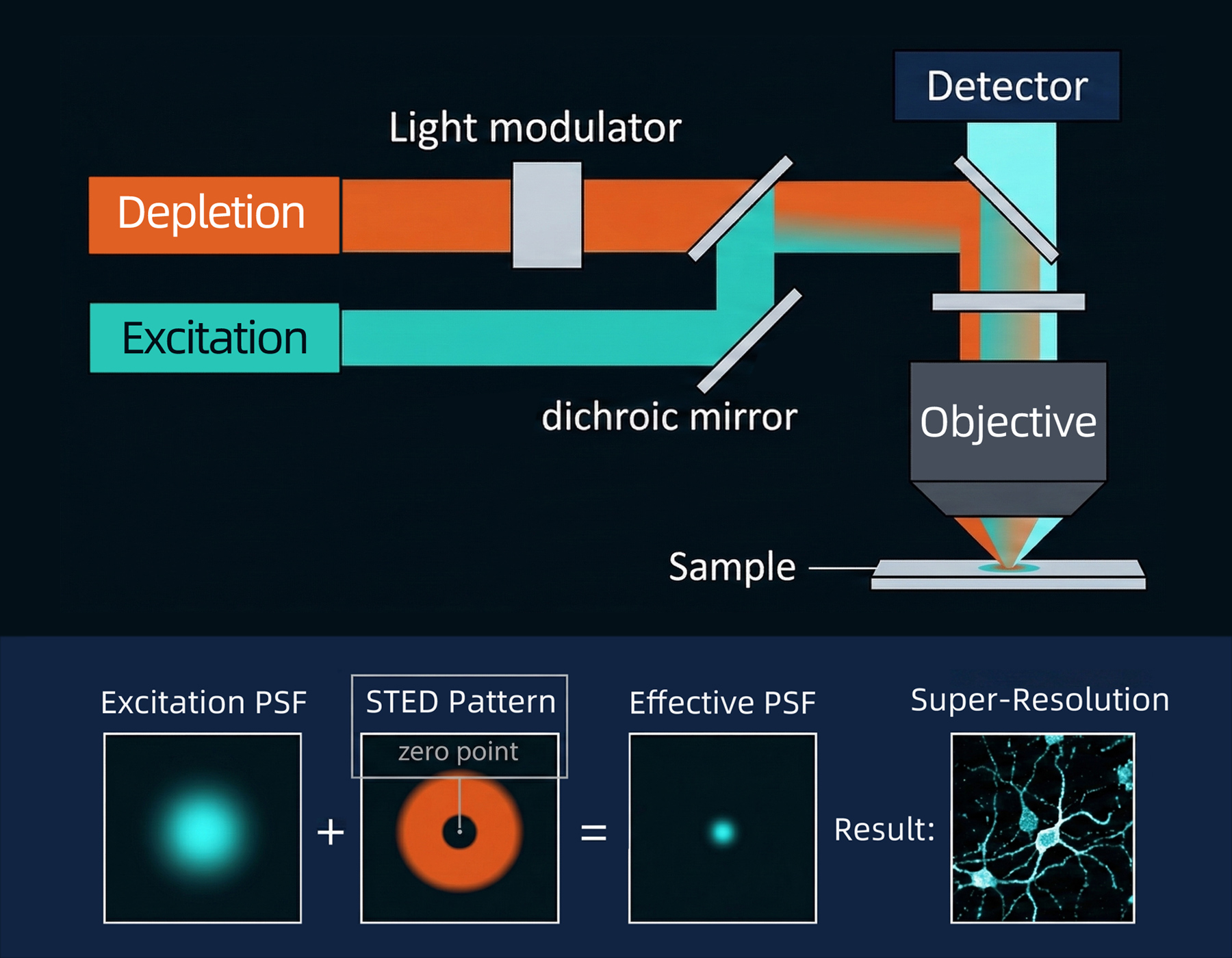
受阿贝衍射极限约束,传统共聚焦显微镜的横向分辨率止步于约 250 nm。 在观察细胞骨架、突触小泡(~40 nm)或病毒颗粒时,往往只能看到模糊的团块—— 蛋白质复合物的亚单元排列、核孔复合物的精细轮廓,均无从分辨。
致微S1 提供高达 40 nm 横向分辨率,使研究人员能直接观察蛋白质复合物的亚单元排列、 核孔复合物的精细轮廓以及纳米材料的表面缺陷,无需复杂样品制备, 在活细胞状态下获取高保真原始数据。
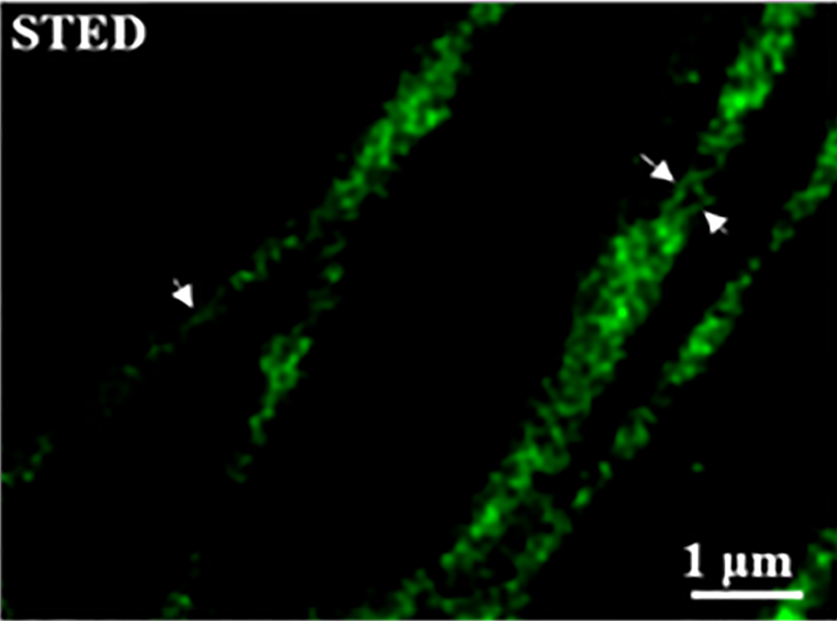
在微管蛋白成像中,STED 模式能清晰分辨出共聚焦模式下无法剥离的平行微丝, 以纳米级精度呈现细胞骨架的真实排布,为结构生物学研究提供高保真原始数据。
移动鼠标 · 查看清晰度对比
 共聚焦
STED
共聚焦
STED
微管蛋白 · Microtubule
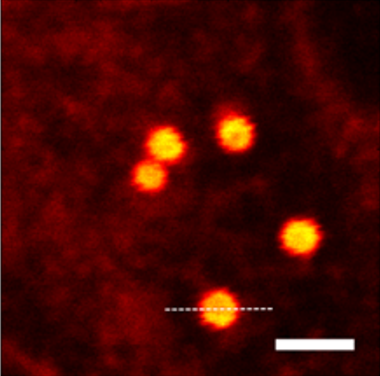 共聚焦
STED
共聚焦
STED
高尔基体 · Golgi Apparatus